我校化学学院张前教授及其研究团队多年来一直从事有机合成方法学研究,建立了多种高效、高选择性C–N键构建新方法,并将新方法运用到各种重要含氮化合物的合成中。相关研究工作受到国内外同行的关注和引用。
该研究团队提出“金属原位进攻与导向基团直接相连的芳烃碳原子”新思路,解决了导向基策略局限于芳烃导向基团邻近位置官能团化的问题,首次实现钯催化芳烃酰胺导向基团远程对位C–H键及对位苄基C–H键的亲核胺化反应(图1),为发展过渡金属催化芳烃区域选择性C–H键转化提供了重要借鉴。
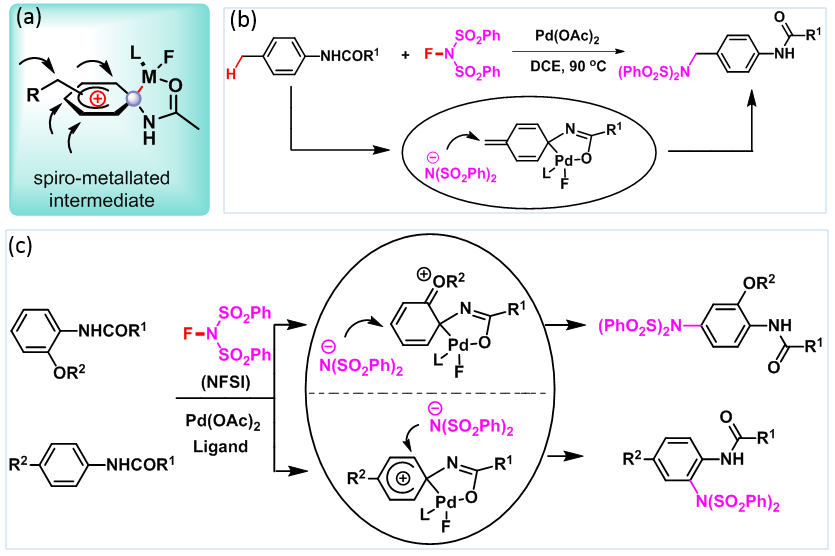
图1:利用“高价金属原位进攻-亲核胺化”新思想,高选择性实现各种C–H键的胺化反应。(a)现场生成的金属杂螺环中间体,(b)导向基对位苄位sp3 C–H的胺化反应,(c)导向基邻位或对位芳烃sp2 C–H的胺化反应。
该团队还提出“温和条件下产生金属配位氮自由基”新策略,开创性地将N-氟代双苯磺酰亚胺用做自由基氮源,创建了烯烃氨氰化反应类型,进而发展了烯烃二氨化、氨氟化、氨氧化、氧化氨化以及炔烃的胺芳化反应和氨化多官能团化串联反应(图2),解决了高选择性自由基胺化的瓶颈问题,为基于氮中心自由基发展不饱和键氨化双/多官能团化反应奠定了坚实的基础。

图2:利用高价金属的氧化还原异构化,在温和条件下产生“金属稳定氮自由基”,高选择性实现自由基胺化反应。(a)金属稳定的氮自由基环中间体,(b)分子间烯烃/联二烯的胺化双官能团化反应,(c)炔烃的胺化多官能团化反应。
此外,该团队建立了一种一价铜与氟正离子氧化剂的高效、可控催化剂体系,实现由苄位C–H键直接高效构建C–N键,突破了已有方法苄位亚甲基C–H键选择性高与苄位甲基的局限,并将该体系成功应用于苯并恶嗪类以及喹唑啉类含氮杂环化合物的合成(图3)。

图3:利用一价铜和氟正离子的催化体系,高选择性实现几种C–H键的活化,构建了系列重要的含氮化合物。(a)一价铜和氟正离子的催化体系现场生成三价铜氟活性物种,(b)苄位sp3 C–H的胺化反应,(c)顺次活化sp2、sp3 C–H键合成苯并噁嗪,(d)顺次活化sp2、sp3 C–H键合成喹唑啉。
该团队在Nat. Commun.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.等刊物上发表研究论文40余篇,创建的C–N键构建新方法,带动了中、美、德、日等国20余个课题组的相关研究工作,系列研究成果荣获2019年度吉林省科学技术奖自然科学一等奖。
科学技术处
2019年11月20日